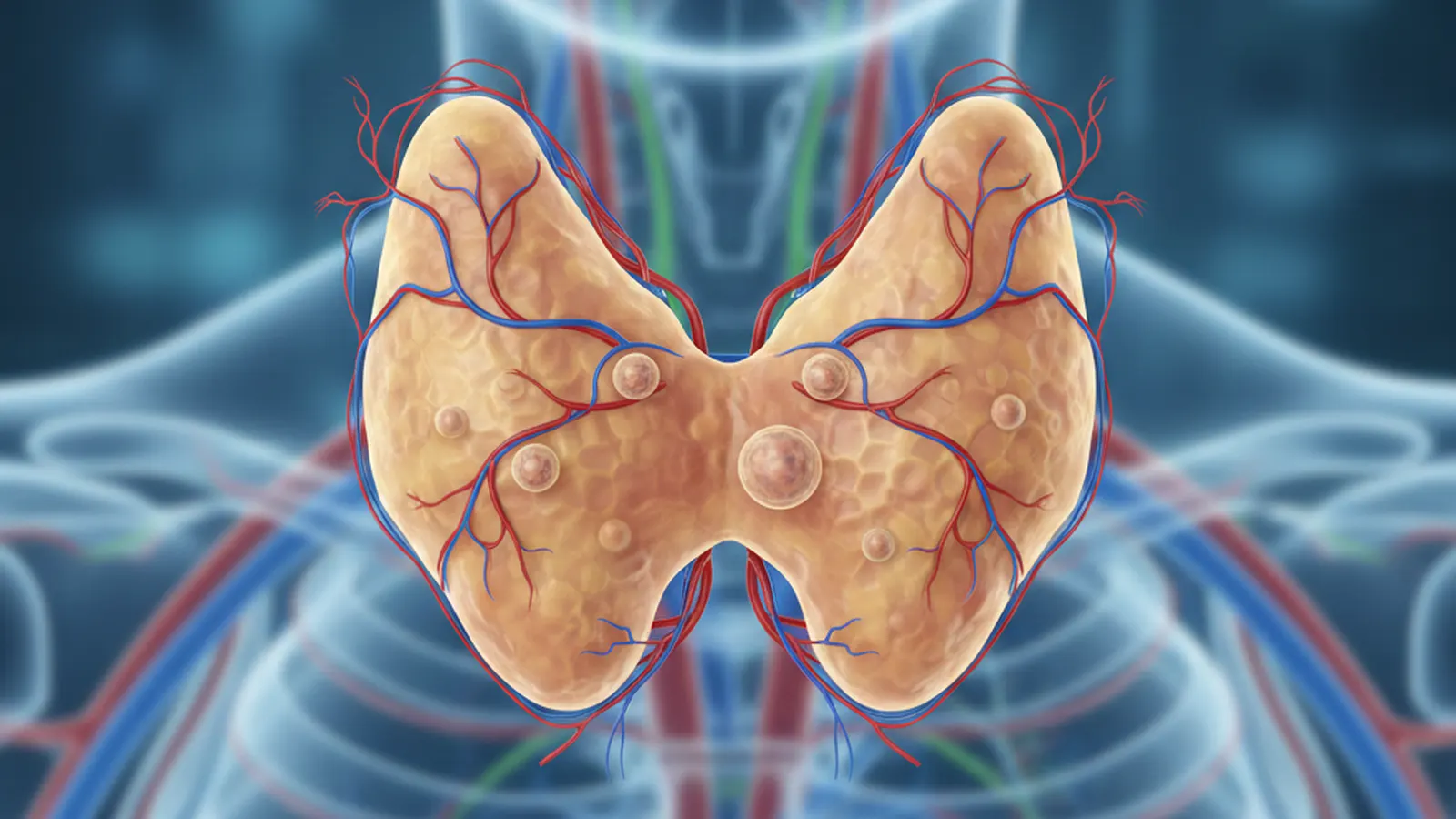
Что такое аутоиммунный тиреоидит Хашимото?
Аутоиммунный тиреоидит Хашимото — это хроническое заболевание, при котором иммунная система ошибочно атакует щитовидную железу. В результате этого процесса щитовидная железа может не вырабатывать достаточное количество гормонов, что приводит к гипотиреозу.
Почему возникает заболевание?
Причины развития аутоиммунного тиреоидита Хашимото до конца не изучены, однако выделяют несколько факторов:
- Генетическая предрасположенность: наличие случаев заболевания в семье может увеличить риск.
- Гормональные изменения: чаще заболевание встречается у женщин, что может быть связано с гормональными колебаниями.
- Экологические факторы: воздействие токсинов и вирусных инфекций может спровоцировать развитие заболевания.
Симптомы заболевания
Симптомы аутоиммунного тиреоидита могут варьироваться от легких до тяжелых, и часто включают:
- Усталость и слабость
- Набор веса
- Чувство холода
- Сухость кожи и волос
- Депрессия и изменение настроения
- Затрудненное сосредоточение
- Увеличение щитовидной железы (зоб)
Диагностика
Для диагностики аутоиммунного тиреоидита Хашимото используются следующие методы:
- Анализы крови: проверка уровня ТТГ, Т4 и антител к тиреопероксидазе (TPO).
- УЗИ щитовидной железы: позволяет оценить размер и структуру железы.
Лечение аутоиммунного тиреоидита Хашимото
Лечение зависит от тяжести заболевания и уровня гормонов щитовидной железы. Основные подходы включают:
Гормонозаместительная терапия
Если уровень гормонов щитовидной железы снижен, назначаются препараты левотироксина для приведения гормонального фона в норму.
Поддержка иммунной системы
Для улучшения состояния могут быть рекомендованы:
- Продукты, богатые антиоксидантами (фрукты, овощи)
- Омега-3 жирные кислоты (рыба, орехи)
- Пробиотики для поддержания здоровья кишечника
Изменение образа жизни
Некоторые изменения в образе жизни могут помочь контролировать симптомы:
- Сбалансированное питание: избегайте продуктов с высоким содержанием глютена и сахара.
- Регулярные физические нагрузки: умеренные упражнения могут повысить уровень энергии.
- Управление стрессом: йога и медитация могут помочь снизить уровень стресса.
Прогноз и возможные осложнения
Своевременная диагностика и лечение аутоиммунного тиреоидита Хашимото помогают контролировать симптомы и улучшать качество жизни. Однако, если заболевание не лечить, оно может привести к осложнениям, таким как:
- Сердечно-сосудистые заболевания
- Психологические расстройства
- Микседема — тяжелая форма гипотиреоза
Заключение
Аутоиммунный тиреоидит Хашимото — это серьезное, но управляемое заболевание. Осведомленность о симптомах, регулярные проверки и правильное лечение помогут вам поддерживать здоровье и качество жизни на высоком уровне.